DISQUES de VALENCE et de STRUCTURE
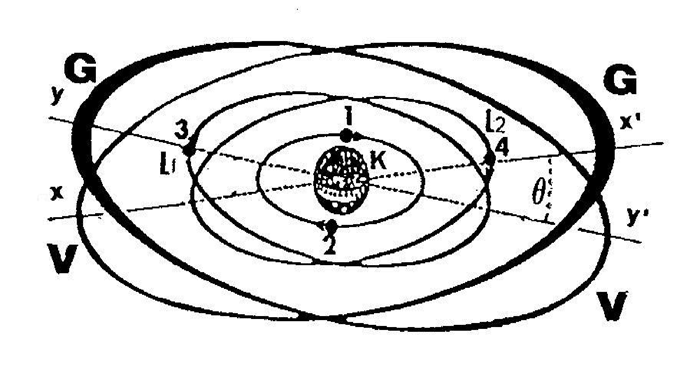
Les ÉLECTRONS (1 et 2) saturent l'orbite (k) qui se prolonge par un DISQUE DE STRUCTURE non représenté.
Les électrons (3 et 4) occupent chacun l'une des orbites L1 ou L2, lesquelles se prolongent en un DISQUE DE VALENCE présentant un arc (G) de forte résistance face à la pénétration d'un disque de valence d'un atome qui voudrait s'y lier. Diamétralement à l'opposé de (G) il y a un arc (V) dit de valence de faible résistance pour l'atome qui voudrait s'y lier, comme dans une structure cristalline de la figures ci-essous.

UN DISQUE DE VALENCE prolonge une orbite sur laquelle gravite un seul électron. Ce disque est apte à se lier avec le même disque d'un autre atome.UN DISQUE DE STRUCTURE prolonge une orbite saturée par deux ÉLECTRONS. Ce disque ne peut se lier à aucun autre.
COMMENT SE FORMENT LES DISQUES ?
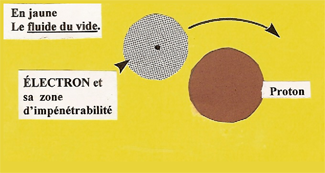 |
EXEMPLE DE L'ATOME D'HYDROGÈNEL'ÉLECTRON minuscule ne heurte pas directement l'énorme PROTON ; sa sphère d'impénétrabilité roule à la surface de celui-ci. Par attraction, l'ÉLECTRON incurve sa trajectoire. Parfois, il s'enroule autour du PROTON et forme avec lui un ATOME d'Hydrogène. |
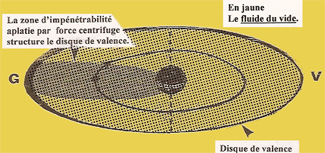 |
Dans ce cas, la sphère d'impénétrabilité en circonvolution autour du noyau, sous l'action des forces centrifuges s'allonge en diminuant d'épaisseur et décrit un disque de valence L'atome d'hydrogène avec son disque de valence est capable de se lier à un autre ATOME. |
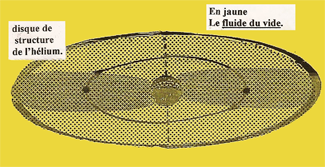 |
DANS L'ATOME D'HÉLIUM qui possède 2 unités (q+) un nouvel ÉLECTRON neutralise la seconde charge (q+) du NOYAU et sature la première orbite. Deux ÉLECTRONS sur une même orbite génèrent un disque de structure incapable de se lier à un autre ATOME. |
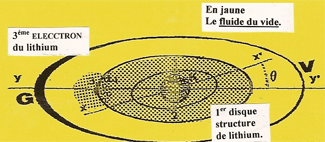 |
L'ATOME DE LITHIUM possède 3 unités (q+) d'électricité sur son NOYAU. Le troisième ÉLECTRON en se positionnant, sur l'axe (yy') à la limite du disque de structure précédent, neutralise la troisième charge (q+) du NOYAU |
 |
Sous l'action des forces centrifuges la zone d'impénétrabilité de ce troisième ÉLECTRON s'allonge en diminuant d'épaisseur et formera un disque de valence qui n'est pas représenté pour ne pas brouiller le dessin. |
Dans les atomes complexes, les ELECTRONS se répartissent sur des orbites successives ; les plus externes sont parfois occupées par un seul ÉLECTRON qui est à l'origine d'un disque de valence. Dans tous les autres cas : deux ELECTRONS, jamais plus, en opposition de phase saturent une même orbite dont le role n'est que structurel.
Dans les atomes complexes
On distingue, deux sortes d'ELECTRONS :
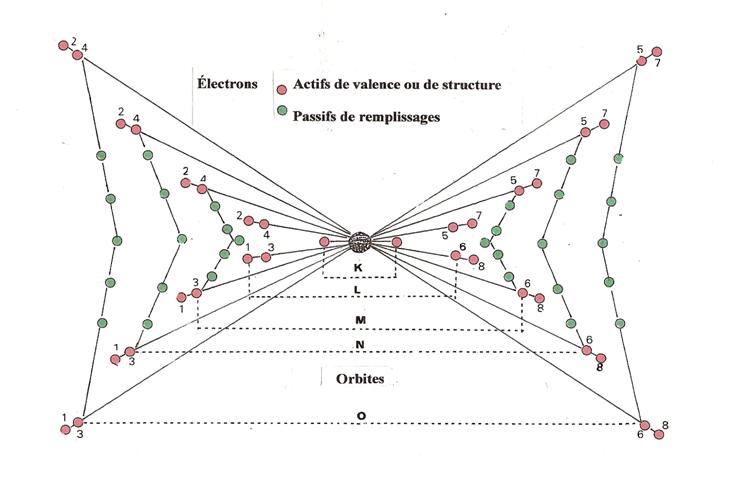
1 - Les électrons actifs (en rouge) exercent deux fonctions différentes :
les uns, de valence ; ce sont ceux ( 4 au maximum par niveau) qui, seuls sur une orbite, génèrent un disque de valence.
. les autres, de structure ; ce sont ceux qui, deux par deux, saturent jusqu'à 4 orbites par niveau et génèrent un disque de structure.
ATTENTION un disque de structure compte 2 électrons
2 - Les électrons passifs (en vert) glissent
entre les disques de structure des différents niveaux : jusqu'à (10), au
niveau (Mp) ; jusqu'à (10 + 14), aux niveaux (Np et Op). Leur rôle se limite à compenser une
quantité (q+) d'électricité.
Certains sont instables et peuvent être passifs ou actifs.
GÉNÉRALITÉS
On distingue, dans les atomes complexes, deux sortes d'ELECTRONS :
A - Ceux dit actifs ont deux fonctions :
- a - Les ELECTRONS de valence occupent chacun une orbite différente et génèrent un disque de valence capable de se lier au disque d'un autre atome.
- b - Les ELECTRONS de structure, deux par deux, saturent l'orbite sur laquelle ils sont en opposition de phase. Cette orbite saturée ne peut plus se lier à celle d'un autre atome, mais devient un élément de structure de l'atome.
B - Ceux dits passifs n'ont aucune fonction dans l'atome si ce n'est de compenser une unité (q+) de la charge électrique nucléaire. Ces ELECTRONS passifs glissent entre les disques de structure des niveaux inférieurs :
- - au niveau (Mp), on peut en compter jusqu'à 10
- - aux niveaux (Np et Op), jusqu'à (10 + 14)
Sur des tableaux en fin de rubrique, vous trouverez la répartition des ELECTRONS dans les atomes des 99 éléments chimiques qui se trouvent dans la nature. Au-delà des deux premiers niveaux (K et L), où les ELECTRONS sont tous actifs. Sur les niveaux suivants, ils peuvent être :
- - actifs, c'est-à-dire de valence ou de structure ; leur nombre est inscrit dans les colonnes (Ma, Na, Oa, Pa et Qa) ;
- - passifs, leur charge électrique sert uniquement à compenser un nombre égal de charges protoniques ; leur nombre est inscrit dans les colonnes (Mp, Np, Op, et Pp).
Si le rôle des ELECTRONS est indéfini, c'est-à-dire qu'ils peuvent être, selon les circonstances, actifs, de valence ou de structure ou bien passifs, leur nombre est inscrit entre deux colonnes. Prenons quelques exemples :
- - Dans un atome de CHROME (z = 24), les 18 premiers ELECTRONS saturent les niveaux (K, L et Ma) :
- - quatre peuvent se placer chacun sur une orbite (Na) et deux autres sur deux orbites (Oa), et l'atome a (6) valences.
- - quatre peuvent se placer chacun sur une orbite (Na) et trois passifs tomber en (Mp) ; l'atome est trivalent.
- - quatre peuvent saturer deux orbites (Na) et, deux sur chacun une orbite, génèrent deux disques de valence ; l'atome est bivalent.
- - Dans un atome de ZINC (z = 30), les 18 premiers ELECTRONS saturent les couches (K, L et Ma). Les 10 autres saturent la couche passive (Mp). Les deux derniers gravitent sur chacun une orbite (Na). L'atome est bivalent.
- - A partir du XENON (z = 54), 34 ELECTRONS saturent les niveaux (K, L, Ma, Na et Oa). 10 sont tombés dans le vide (Mp) et 10 autres dans le vide (Np). Le XENON est un gaz inerte sans disque de valence.
- - Au-delà de l'atome d'HAFNIUM, les ELECTRONS supplémentaires se retrouvent en (Pa et Qa) ou tombent dans le vide (Op), sauf pour le PLATINIUM (z = 78) dont les 68 premiers ELECTRONS saturent les niveaux (K, L, Ma, Na et Oa) et les vides des niveaux (Mp et Np) et, parmi les 10 derniers : 6 glissent dans le vide (Op) et quatre occupent chacun une des orbites (Pa). Cet atome est quadrivalent, à moins que deux ne se groupent en opposition de phase sur la même orbite (Pa), ce qui rend l'atome bivalent.
- - Dans l'atome de RADON (z = 86), tous les niveaux (K, L, Ma, Na, Oa et Pa) sont saturés et les vides (Mp, Np et Op) comblés, de sorte que l'atome est inerte.
Les ELECTRONS des atomes suivants n'ont d'autre fonction que d'occuper, seul ou par deux, les quatre orbites (Qa) ou de glisser dans le vide (Pp).
La dernière colonne à droite du tableau (pages 60 et 61) comporte un symbole de deux lettres qui définit la propriété physique de chaque atome : A (alcalin) ; AC (Actinide) ; AT (alcalino-terreux) ; H (halogène) ; I (gaz inerte) ; M (métaux) ; NM (non métaux) et TR (terres rares).
Modifications des structures électroniques
Lorsqu'un PHOTON heurte un ELECTRON d'un atome complexe, avec une énergie (Wa) supérieure à celle (Wi) dite d'ionisation, l'ELECTRON de masse (me) est expulsé de l'atome avec une vitesse (v) telle que
Wx > Wi → Wx = Wi + (me . v² / 2)
Dans un atome complexe, chaque ELECTRON est indépendant, c'est dire qu'il possède sa propre énergie (Wi) qui varie de l'un à l'autre en fonction de son environnement électrique.
L'atome privé d'un ELECTRON devient à cation, dont les dimensions externes sont plus réduites que celles de l'atome entier.
Un atome peut perdre un ou plusieurs électrons. Les rayons (R) des cations et les énergies (Wi) d'ionisations sont représentés par les divers symboles ci-après :
| Rayon de l'ATOME | Énergie d'ionisation d'un ATOME |
| R1 = dans son état stable en Å | W1 = première ionisation en eV |
| R+1 = privé d'un ELECTRON de valence en Å | W2 = deuxième ionisation en eV |
| R+2 = privé de 2 ELECTRONS de valence en Å | W3 = troisième ionisation en eV |
| R+3 = privé de 3 ELECTRONS de valence en Å | Rw = Résistance à 20°C en µ;Ω/cm |
Structure électronique des atomes dans leur état fondamental
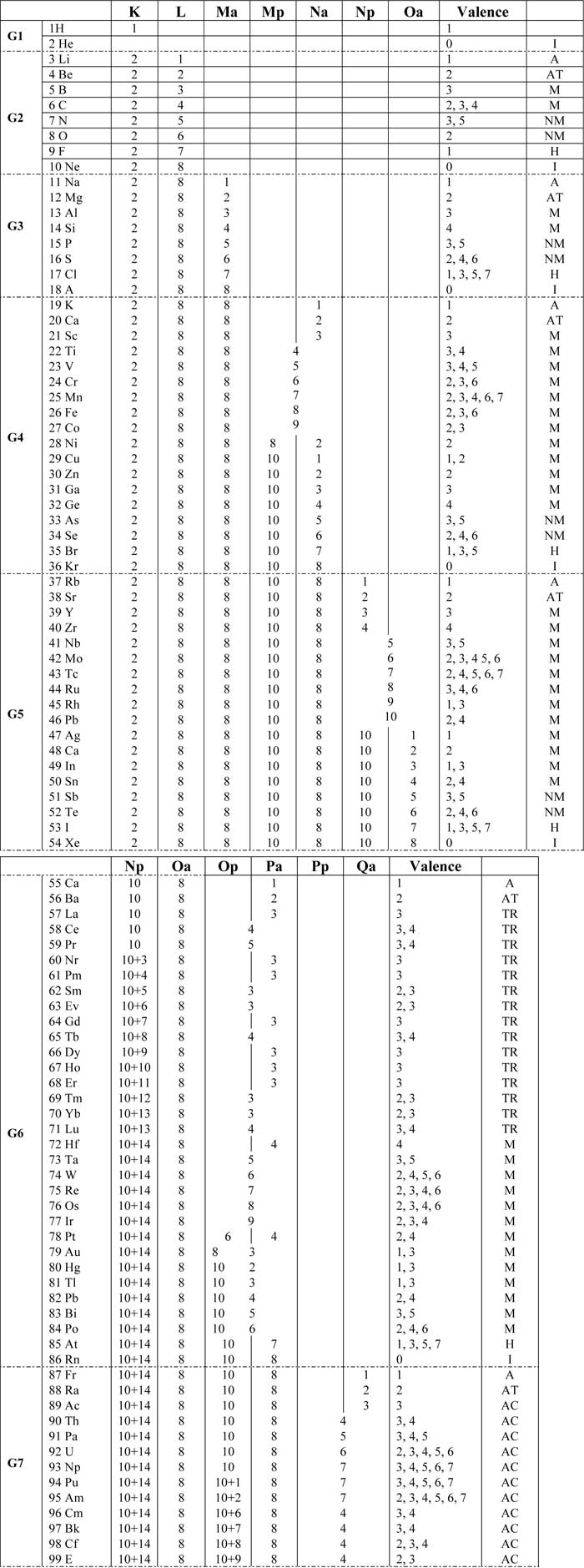
Sur le tableau ci-dessus :
Éléments ALCALINS (sont marqués A)
Eléments ACTINIDES sont marqués AC)
Éléments ALCALINO-TERREUX (marqués A)
Éléments HALOGENES (marqués H)
Gaz rares ou inertes (marqués I)
Les métaux (marqués M)
Les non métaux (marqués NM

