LES ARN
DESCRIPTION DES ARN
L'acide ribonucléique (ARN) est un polymère similaire à l'ADN, aussi bien en terme structurel qu'en terme fonctionnel (matérialisation et traitement de l'information génétique). Il y a quatre différences par rapport à l'ADN : - le sucre désoxyribose est remplacé par un ribose. Ce changement explique l'instabilité des molécules d'ARN, car les deux fonctions alcools géminés sont susceptibles d'hydrolyse alcaline et acide tandis que le désoxyribose de l'ADN y est insensible ; |
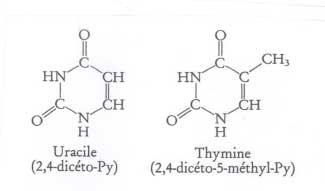 |
- la base thymine est remplacée par un uracile;
- l'ARN est généralement simple brin, sauf chez quelques organismes tels les rétrovirus, tandis que l'ADN est double brin avec une structure en double hélice ;
- l'ARN est court (50 à 5.000 nucléotides et non pas des millions, comme dans l'ADN).L'uracile
est moins coûteux
à produire pour les organismes vivants que la thymine, mais se convertit
lentement en cytosine. Ce serait pour cette raison que l'ARN a de l'uracile et l'ADN de la thymine : la cellule
produit beaucoup d'ARN mais ne le conserve pas, c'est donc le coût de production qui prime sur la stabilité
de l'information. A l'inverse, l'ADN doit conserver une information longtemps mais n'est produit que rarement
(lors de la division cellulaire), c'est donc la stabilité qui prime sur le coût.
D'un point de vue évolutif, certains éléments permettent de penser que l'ARN serait antérieur à l'ADN comme support de l'information génétique, ce qui expliquerait ses fonctions plus étendues et sa généralisation. L'ADN serait apparu plus tard et n'aurait supplanté l'ARN que pour le rôle de stockage à long terme, en raison de sa plus grande stabilité. Notons ici que cette stabilité est conférée par la disparition d'une fonction alcool (-OH, oxy) au niveau 2' du ribose (D de ADN signifie désoxyribonucléique, i.e. ayant perdu une fonction oxy au niveau du ribose). De plus, la stabilité temporelle de l'information génétique est aussi liée au fait que l'ADN soit bicaténaire (double brin) : en effet, si une mutation se produit sur un brin de l'ADN, la cellule peut, grâce à des mécanismes de réparation, corriger cette erreur en se basant sur la complémentarité des brins.
ARN PRE-MESSAGER ou ARNpm
ADN est constitué de deux brins :
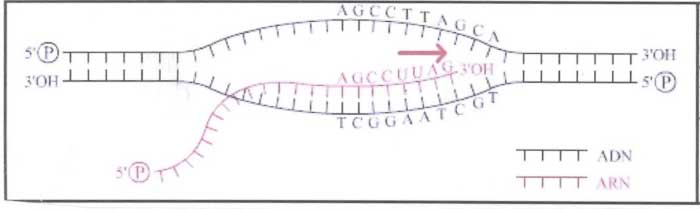
- l'un, non codant, est orienté de 5' vers 3' et est constitué de codons ;- l'autre, le brin codant, vient de 3' vers 5' ; il est constitué d'anti-codons de sorte que son complément, l'ARNpm, sera fait de codons.
En réalité, l'ADN pré-messager est constitué de multiples fragments ; les plus nombreux donneront des GENES codants puis des PROTEINES ; d'autres des éléments fonctionnels comme les (ARN transfert), les (ARN ribosomaux), des fragments enzymatiques, des introns et des exons.
La reconnaissance de ces différents fragments nécessite la présence de repères appelés
promoteurs. Ceux-ci correspondent à une région non transcrite de l'ADN, généralement
juste en amont du début de la région transcrite. Certaines séquences du promoteur (surnommées
boîtes
) ont une importance particulière dans ce processus, essentiellement parce que ces séquences
sont reconnues spécifiquement par différentes protéines appartenant au complexe
d'initiation.
Parmi les boîtes
, la plus importante est celle dite (TATA) parce que riche en Thymine et Adénine.
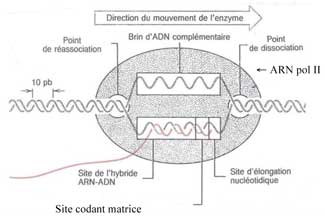
Grâce à un jeu de protéines qui reconnaît cette boîte (TATA) et y procède à la séparation des deux brins de l'ADN ; un ARN pol II peut se placer juste après et procéder à la TRANSCRIPTION.
 |
L'acide ribonucléique (ARN) est un polymère similaire à l'ADN, aussi bien en terme structurel qu'en terme fonctionnel (matérialisation et traitement de l'information génétique). Il y a quatre différences par rapport à l'ADN : - le sucre désoxyribose est remplacé par un ribose. Ce changement explique l'instabilité des molécules d'ARN, car les deux fonctions alcools géminés sont susceptibles d'hydrolyse alcaline et acide tandis que le désoxyribose de l'ADN y est insensible ; |
ARN CODANT POUR LES GENES
L'ARN pm (pré-messager) tel qu'il est traduit n'est pas apte à synthétiser des protéines. Il doit subir des modifications qui répondent à plusieurs impératifs (augmentation de la demi-vie, modification de la séquence). Toutes ces modifications sont réalisées au fur et à mesure de la progression de la synthèse du préARNm dans le nucléoplasme. Il existe trois grands types de modifications, catalysées chacune par des enzymes de nature protéique ou ribonucléique.
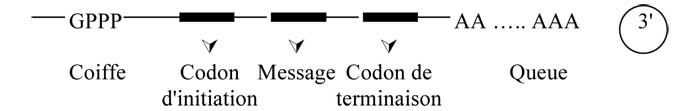
A - Structure de la coiffe d'un ARN
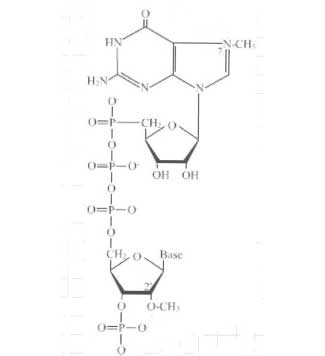 |
La coiffe se caractérise par l'ajout d'un nucléotide à guanine (G) à l'extrémité 5' du brin d'AEN. Ce nucléotide à guanine est relié à la chaîne nucléotidique par une liaison inhabituelle : au lieu d'être reliés par une liaison ester-phosphorique entre le groupement OH porté par le carbone 3' du ribose du nucléotide à guanine et l'acide phosphorique alpha du premier nucléotide de l'ARN natif, les deux nucléotides sont reliés par une liaison anhydride d'acide entre les acides phosphoriques des deux nucléotides. Par la suite, le cycle imidazole de la guanine terminale est méthylé sur son azote 7. Par ailleurs, le ribose du premier nucléotide de l'ARN natif est méthylé sur l'oxygène porté par le carbone 2'. Ce peut également être le cas du nucléotide suivant. |
B - L'addition d'une queue polyA en 3'
Le site de polyadénylation est codé au niveau du gène. Le site de clivage déterminé par le dinucléotide CA est entouré par une séquence AAUAAA très conservée située 10 à 30 nucléotides en amont du site de clivage, et par une séquence DES (Down Stream Element) riche en U ou en GU situé à une trentaine de nucléotides en aval du site de clivage. La séquence AAUAAA est reconnue spécifiquement par un complexe protéique appelé CPSF (Cleavage and Polyadenylation Specific Factor), et la séquence DES par un complexe CstF (Cleavage Stimulation Factor). Ces deux complexes et d'autres composants, comme l'ARN polymérase II et la poly(A) polymérase (PAP), vont interagir en formant le complexe de clivage qui va cliver la molécule de préARN au niveau du site de clivage.
Il faut noter que la queue n'est pas codée par la matrice ADN. Cette queue confère de la stabilité à l'ARNm et se perd au fur et à mesure qu'il est traduit. Les gènes ainsi constitués gagnent le cytoplasme.
C - L'excision-épissage de l'ARN pré-messager en ARN messager
Alternance d'exons (parties codantes du gène) et d'introns (parties non codantes, bornées par des séquences
de bases spécifiques : 5'GU et 3'AG), ils sont d'abord intégralement recopiés dans l'ARNpm,
puis subissent une opération Chez les eucaryotes, les archéobactéries et les cyanobactéries,
les gènes sont morcelés : constitués d'une d'excision des introns (ainsi que celle,
parfois, de petits morceaux d'exons) suivi d'un épissage (splicing), c'est-à-dire la réunion
bout à bout des exons restants qui constituent l'ARNm. Ce remaniement se déroule au fur
et à mesure de la progression de la transcription.L'excision des introns s'opère par
l'entremise d'une formation dite en lasso
(Figure ci-dessous).
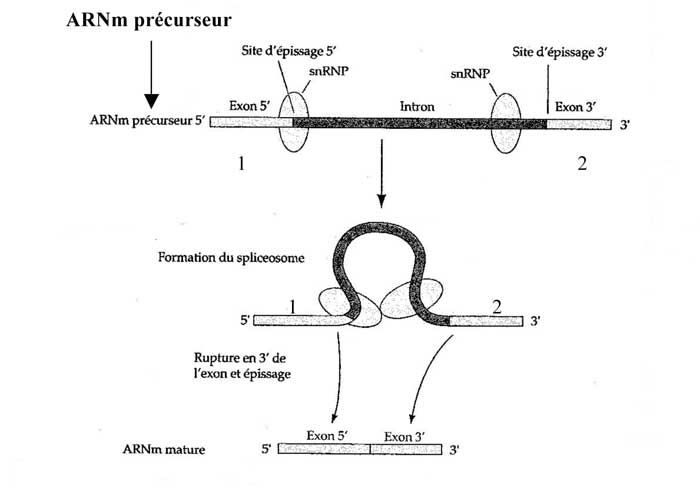
D - Excision de l'intron par formation d'un lasso
L'excision-épissage est réalisée par réaction d'un nucléotide à adénine (A) situé dans l'intron avec un nucléotide à guanine situé en 5' de l'intron. Cela entraîne la séparation de l'intron d'avec l'exon 1 (situé en amont) et la formation d'une structure en lasso interne à l'intron. Ensuite, l'extrémité 3' de l'exon 1 réagit avec l'extrémité 5' de l'exon 2 permettant l'épissage des deux exons et la libération du lasso qui sera dégradé par des ribonucléases.
Il faut préciser que plusieurs types d'INTRONS sont connus pour être utiles ; certains codants pour des protéines qui leur permettent de s'insérer ailleurs dans le génome, on a donc un gène caché à l'intérieur d'un autre gène.
ARN MESSAGER NON CODANT
A - Les ARNt
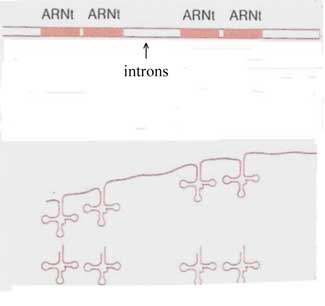 |
Tout l'ADN n'est pas transcrit en (ARNpm) : Une partie est transcrite par un (ARN pol III) en plusieurs éléments :
|
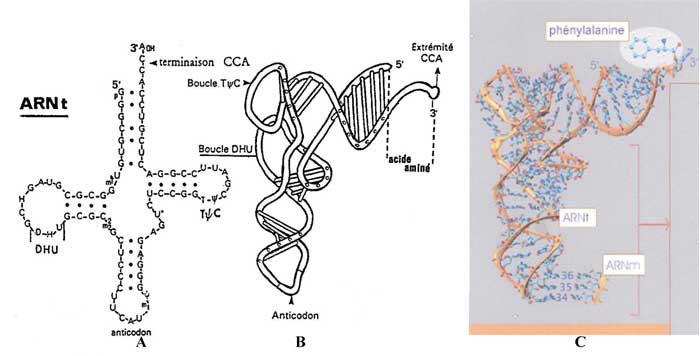
Les ARNt sont constitués d'un peu moins d'une centaine de nucléotides et adoptent une structure caractéristique résultant de nombreux appariements entre bases.
A leurs extrémités 3', tous les ARNt portent la séquence 5' CCA 3'. C'est à cette extrémité de l'ARNt qu'est attaché l'acide aminé par une aminoacyl-tARN synthétase. Chaque aminoacyl-ARNt synthétase reconnaît un unique acide aminé et l'ARNt correspondant. Chaque ARNt possède aussi une boucle contenant l'anticodon qui va s'apparier avec le CODON correspondant sur l'ARN messager.
Comment l'ARNt se combine-t-il correctement avec l'acide aminé ? C'est grâce à un enzyme d'activation ou aminoacyl-ARNt synthétase spécifique de chaque acide aminé.
Celui-ci réagit d'abord avec une molécule d'acide aminé et une molécule d'ATP, produisant une liaison riche en énergie AMP-acide aminé qui reste liée à l'enzyme. L'énergie vient de la rupture des liaisons de l'ATP. L'enzyme catalyse le transfert de l'acide aminé à partir de l'AMP vers l'extrémité 3' du NUCLEOTIDE terminal d'ARNt, où il est maintenu par une liaison relativement riche en énergie.
Sur la figure ci-dessus C, l'ARNt porte l'acide aminé phénylalanine (F) en positionnant son anticodon face aux CODONS de l'ARNm marqués 34, 35 et 36.
B - Les ARNi (interférents)
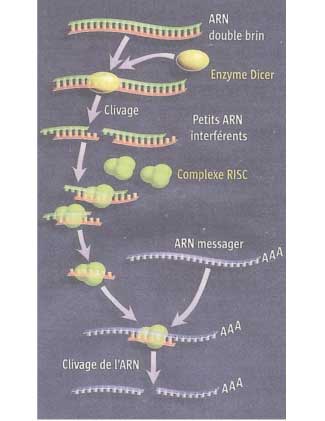 |
Selon les biologistes, à l'origine de la vie, de petits ARNi de quelque 15 de nucléotides (soit 5 CODONS) venaient se coller aux ARN viraux, neutralisant ainsi leur reproduction Les plantes et les invertébrés s'en servent toujours ainsi. Chez les humains, les ARNi allument ou éteignent des gènes en fonction des besoins de l'organisme. Depuis 1990, des biologistes cherchent à synthétiser des ARNi avec deux objectifs : lutter contre le dérèglement génétique et agir contre certains agents infectieux. Progressivement, les scientifiques se sont aperçus qu'ils avaient négligé un potentiel et ont repris toutes les petites séquences d'ARN qu'ils avaient toujours ignorées, en se demandant, pour chacune, à quoi elles pouvaient leur servir. Andrew PIRE et Craig MELLO ont été, en 2006, récompensé du Prix NOBEL pour avoir expliqué comment un brin ARN minuscule vient se fixer sur un gène ARNm (messager) pour l'annihiler. |
C - Les ribosomes
Différentes parties notées en (S) = SVELDBERG, unité de poids propre aux grandes molécules :
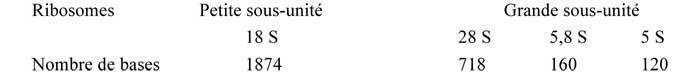
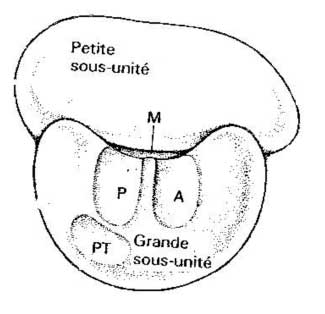 |
Dans le NOYAU des EUCARYOTES, on trouve des NUCLEOLES qui contiennent un ADN. Celui-ci, à l'aide de ARN pol I, transcrit des ARNr (28 S et 5,8 S) qui se groupent pour former la grande sous-unité d'un RIBOSOME et un ARNr 18 S qui, à lui seul, constitue l'armature de la petite unité d'un RIBOSOME. Les squelettes des deux sous-unités d'un RIBOSOME se libèrent des NUCLEOLES et quittent le NOYAU pour se retrouver dans le cytoplasme où ils s'habillent de protéines où également la grande sous-unité ajoute à sa structure un ARNr 5 S qui provient directement d'une fraction de l'ARNpm (pré-messager) transcrit par l'ARN pol III. |
De leur côté, des protéines en provenance du cytoplasme finissent de garnir les deux parties des ribosomes. Ceux-ci définitivement habillés migrent dans le cytoplasme où les deux sous-unités commencent leur activité de synthèse des protéines.
Souvent, plusieurs ribosomes traduisent simultanément un même gène sur lequel ils progressent comme sur un rail.
Quelle que soit la forme de vie, les Ribosomes ont tous une architecture comparable et leurs composants homologues remplissent les mêmes fonctions, ce qui suggère qu'ils seraient apparus tôt au cours de l'évolution et qu'ils seraient issus d'un même ancêtre.
Selon certains biochimistes canadiens le ribosome à l'instar des autres molécules d'ARN primitives simples proviendrait d'un processus d'assemblage spontané. Comme d'autres ARN ils se seraient assemblés au hasard à partir de motifs structuraux fondamentaux sans but prédéterminé.
A l'origine, le ribosome était a 100% composé d'ARN, les protéines sont apparues plus tard. D'ailleurs il est intéressant de noter que la majorité des protéines se localisent uniquement à la surface du ribosome et pas du tout proche du centre catalytique
Serge Steinberg, professeur de biochimie à l'Université de Montréal précise : « Même si le ribosome est une structure complexe, il présente une hiérarchie très nette qui s'est dégagée des principes chimiques fondamentaux »

